![]()
En:
El Portal Indispensable
________________________________________
La última frontera de la química
Escrito por Kanijo en Astrobiología, Astronomía, Química
19 de enero 2010

En el espacio, los compuestos pueden gestarse en el polvo y gas de regiones tales como el centro galáctico de la Vía Láctea y la zona de alrededor de activa formación estelar. Composición de radio- infrarrojo submilimétrico de Adam Ginsburg/Univ. de Colorado en Boulder y cortesía NRAO, Associated Universities, Inc.
El paisaje podría ser el guión de una película post-apocalíptica. Es un entorno extremo, barrido por intensa radiación, feroces vientos y ondas de choque procedentes de violentas explosiones. Aún en esta desolación, una especie perdura. No sólo están las caras comunes y corrientes, hay algo más, sugieren las pruebas, una variopinta tripulación: bandas galácticas que harían encogerse a Mad Max. Algunas están adornadas con metal; otras son radicales impacientes por reaccionar, recorridas con cargas positivas y, según muestra una nueva investigación, incluso negativas.
Estas especies son las moléculas del espacio, los compuestos químicos cósmicos que moran en el vacío mundo de tinieblas entre las estrellas. Tras décadas catalogando estos especímenes químicos, los científicos están recibiendo ahora un torrente de datos que puede llevar a una mejor comprensión de las reacciones que crean y destruyen los compuestos cósmicos.
Los investigadores están centrándose en las especies reactivas renegadas, incorporando a estos actores en modelos de los ciclos de vida que gobiernan la química espacial. Los eléctricos personajes pueden desempeñar grandes papeles interestelares en la formación de moléculas complejas más grandes – y tal vez ser los principales candidatos para la vida.
Los habitantes químicos del espacio están íntimamente vinculados a la formación estelar y el gran ciclo cósmico que da lugar a los sistemas planetarios. Los científicos esperan que la exploración química del medio interestelar con su gas y motas de polvo revele pistas sobre el nacimiento y evolución de las galaxias, estrellas y planetas. Ademas de este objetivo está la emoción de retirar la envoltura química, estudiando una frontera no cartografiada. Es una empresa a la que ayudarán nuevos telescopios, novedosas técnicas de laboratorio y teorías astronómicas y aún más cosas.
“Estamos intentando comprender y atacar los principios químicos fundamentales”, dice el astroquímico Anthony Remijan del Observatorio Nacional de Radio Astronomía (NRAO) en Charlottesville, Virginia. “Estamos tomando los principios químicos más fundamentales que conocemos y amamos y vemos si se mantienen en las extremas condiciones del espacio interestelar”.
Vagabundos cósmicos
Los hostiles entornos del espacio proponen retos tanto a las moléculas que viven allí como a los científicos que las estudian. El espacio es, bueno, espacioso, haciendo difícil que los compuestos se conecten. Las temperaturas son extremas y las presiones pueden ser extremadamente bajas. En el espacio, algunas moléculas dan tumbos hacia regiones desoladas en forma de gas; otras moran y reaccionan en trocitos de polvo helado – estilos de vida difíciles de ver en la Tierra.
“En la Tierra, siempre hay fase líquida, fase líquida y fase líquida”, dice el químico Brooks Pate de la Universidad de Virginia, también en Charlottesville. “Pero eso es algo que no tienes en el espacio. Todo es fase gaseosa y química de superficie. Esto lleva a un tipo de química completamente distinto que no ves en las condiciones terrestres. No es como si hubiese leyes de la física nuevas. Son las condiciones físicas donde tienen lugar las reacciones las que son bastante diferentes”.
La química terrestre a menudo tiene lugar en solución, donde ninguna molécula está nunca aislada. Pero en el medio interestelar, vastas distancias separan las moléculas – si dos personas estuviesen a una distancia proporcional, una estaría en la Tierra y otra en la Luna.
Una descripción emergente revela cómo las moléculas en el espacio usan llamativas cargas para atraerse entre sí a distancia. Las colisiones con partículas, luz estelar ultravioleta y rayos cósmicos, por ejemplo, pueden cargar una molécula. Hasta hace poco, sólo se habían detectado especies neutras y positivas. Los investigadores pensaron que la radiación arrancaría rápidamente a una molécula los electrones extra que confieren carga negativa. Pero ahora se ha encontrado un puñado de moléculas con cargas negativas.
Quedar adornado con cargas da a las especies una ventaja, haciéndolas visibles desde lejos o permitiéndoles atravesar el hielo. La mayor parte de las moléculas terrestres son neutras. No destacan. Estas cenicientas químicas tienen que estar a pocos nanómetros de otras para interactuar, dice Pate. Pero las especies altamente reactivas del espacio pueden arrastrarse unas hacia otras desde cientos de nanómetros de distancia.
Aunque estas especies suenan a vagabundos cósmicos, existen en la Tierra, dice Pate, pero en concentraciones muy bajas y a menudo sólo en el camino de convertirse en otra cosa. En ese aspecto, la química del espacio es como mirar la química de la Tierra a cámara lenta. En la Tierra podría existir una molécula durante un nanosegundo antes de colisionar con otra molécula. En el espacio el tiempo entre colisiones puede ser de semanas o años. Una molécula es más probable que encuentre una compañera si está decorada con cargas.
Sólo el fuerte sobrevive
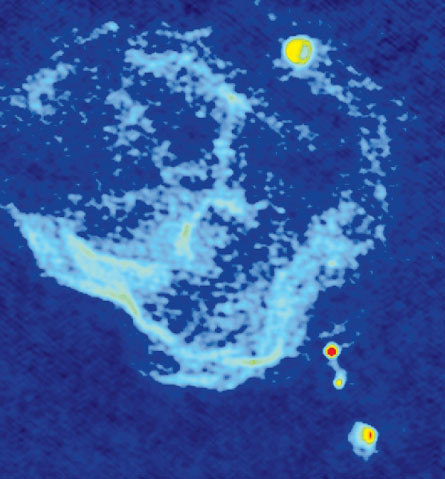
Legiones de moléculas, incluyendo el azúcar simple glicoaldehído, han sido detectadas en una nube molecular (el azul indica emisiones de radio más débiles, las rojas más fuertes) en la constelación de Sagitario. Cortesía de NRAO, Associated Universities, Inc.
Las pruebas sugieren que las frías y oscuras nubes que moran en el medio interestelar son la sala de tatuaje eléctrico del cosmos — puntos calientes para la decoración de cargas. Estas nubes ofrecen un refugio para los pocos resistentes que sobreviven a los choques y radiación del medio interestelar.
El polvo y gas interestelar se crea localmente — naciendo de las estrellas moribundas. Durante gran parte de sus vidas, las estrellas queman hidrógeno creando helio. Después de que se agote el hidrógeno, el helio se convierte en oxígeno y carbono (si las estrellas son lo suficientemente masivas, sigue fabricando y se forman más elementos). Debido a que hay más oxígeno que carbono en la galaxia, los científicos habían pensado que este carbono no estaría disponible para la química orgánica. Antes sería capturado por el oxígeno, formando monóxido de carbono. Pero en la emisión de algunas estrellas, la proporción de oxígeno-carbono está lo bastante filtrada como para que puedan formarse las cadenas de carbono. La eyección de estas estrellas carbónicas extremas lanza carbono al medio interestelar donde puede alimentar la creación de nubes moleculares ricas en dicho elemento.
Pasar del flujo estelar al difuso medio interestelar es un viaje de la cuna a la tumba para muchas moléculas, dice Scott Sandford del Centro de Investigación Ames de la NASA en Moffett Field, California. Cualquier cosa que vague en este vertedero interestelar experimenta una intensa radiación ultravioleta, bombardeo de rayos cósmicos y ondas de choque que impactan a cualquier cosa que encuentren en su camino. “El medio insterestelar difuso no produce cosas, las reduce”, dice Sandford. “Muchos alfeñiques son eliminados”.
Los trozos de compuestos dispersados en los violentos procesos del medio insterestelar pueden reunirse en nubes junto con las moléculas resistentes extra-grandes, tales como los hidrocarburos aromáticos policíclicos o PAHs. En la Tierra, estos compuestos de seis anillos de carbono fusionados (como la alambrada de un gallinero) son contaminantes relacionados con la combustión, difamados por su naturaleza carcinógena. Pero en el espacio, los PAHs surgen como estrellas químicas, moléculas que pueden contener una buena porción del carbono del medio interestelar.
Es dentro de las nubes interestelares donde mejora la química, dice Sandford. “La luz estelar es bloqueada y de pronto las moléculas ya no se destruyen”, comenta. “Pueden sobrevivir, y entonces tienes más compuestos debido a que hay mucho más material en un área menor”.
La química de las nubes
Muchas de las especies moleculares complejas se encuentran en estas nubes frías y oscuras. Desde que comenzó la búsqueda de moléculas interestelares en la década de 1960, la sintonización de la sinfonía molecular que se vierte desde una región de densas nubes en la constelación de Sagittarius ha revelado una gran cantidad de especies. Muchas son varios átomos fuertes. Una huella nota por nota — el espectro de energía emitido cuando una molécula se retuerce y grita — puede determinarse en el laboratorio, y entonces la firma espectral puede detectarse en el cielo, y viceversa. En abril, un equipo internacional de astrónomos que observaba la región de Sagittarius con el telescopio IRAM de 30 metros en el Pico Veleta en España informó de la detección de metanoato de etilo, el cual ayuda a dar a las frambuesas su sabor afrutado en la Tierra. Y usando el Telescopio Robert C. Byrd de Green Bank en Virginia Occidental, Remijan y sus colegas detectaron acetamida, una de las dos moléculas interestelares con un enlace péptido, la misma conexión que une los aminoácidos, los bloques básicos de las proteínas.
Las pruebas sugieren que las nubes están donde muchos exóticos incondicionales lograron sus galones, dice Eric Herbst de la Universidad Estatal de Ohio en Columbus. Conforme se calientan las nubes, las grandes moléculas neutras pueden formarse a partir de los pequeños precursores cargados, incluyendo, tal vez, la especie negativa recientemente descubierta de C6H-, un anión de cadena de carbono, según informaron Herbst y sus colegas el año pasado en Astrophysical Journal. Incorporar especies negativamente cargadas a los modelos de la química de las nubes oscuras hace que estos sean más precisos al predecir la abundancia observada de ciertos compuestos, según informa el equipo.
Una forma común de lograr su energía en estas especies cargadas es a través del hidrógeno molecular protonado, H3+, dice Pate. Esta molécula de tres átomos de hidrógeno con una carga positiva es uno de los iones más abundantes del universo y se forma cuando el H2 es bombardeado con rayos cósmicos que pueden penetrar en las densas nubes. El hidrógeno molecular protonado es un ácido, ansioso de donar protones a otras moléculas, un regalo que puede ayudar a que tengan lugar reacciones minimizando la curva energética que deben superar las moléculas para llevar a cabo su tarea.
“H3+ puede ser el mejor catalizador del mundo interestelar”, dice Pate.
Las cadenas de reacción que empiezan con el H3+ pueden llevar a un conjunto de especies complejas, señala Herbst, aunque muchas de las reacciones apenas se comprenden. Y cuando el H3+ transfiere un protón, también confiere reactividad. Pate está investigando cómo otra molécula abundante, el metanol, adquiere una actividad de reacción acelerada cuando capta protones extra.
Los PAHs también pueden ser catalizadores que aumentan la formación de hidrógeno protonado, el cual puede a su vez permitir más reacciones, según informaron investigadores de la Universidad de Colorado en Boulder el pasado otoño en Astrophysical Journal.
Pero simplemente lograr unir estas dos moléculas no es suficiente. Las colisiones entre gases pueden romper los enlaces, y distanciar las moléculas (la técnica analítica de la espectrometría de masas depende de esta “disociación por colisión”). Los enlaces también pueden formarse para crear nuevas especies. Pero en el espacio, las moléculas pueden ser esquivas. Dos gases pueden colisionar pero, en lugar de enlazarse, forman un complejo en el cual mantienen sus propias entidades.
Química en el hielo
Si no te van las reacciones entre gases, las especies reactivas también se encuentran en la superficie – o incluso dentro – de los granos de polvo. Los trozos de hollín y silicatos que forman el polvo interestelar pueden desarrollar mantos de hielo de varias capas de grosor. El propio hielo normalmente es agua helada, pero otros compuestos, como el amoniaco, metano y dióxido de carbono, pueden estar presentes. Cuando las temperaturas dentro de una nube caen en picado, los gases pueden condensarse en granos de la misma forma que el hielo se acumula en un congelador, dice el químico Ralf I. Kaiser del Instituto de Astrobiología de la NASA de la Universidad de Hawai en Manoa.
“En la química clásica de instituto, los hielos no tienen química; la química está muerta”, dice Kaiser. Pero los experimentos de Kaiser y otros sugieren que la energía de los rayos cósmicos y los fotones ultravioleta pueden penetrar en estos helados trozos de polvo, generando reacciones incluso en el hielo.
Los mecanismos no están claros, pero los científicos creen que estas reacciones podrían tener lugar cuando los fotones excitan el material sólido, creando túneles a través de los cuales los electrones pueden viajar para encontrarse con las especies encerradas en el hielo. O las especies en fase gaseosa pueden aterrizar en un grano de hielo y conectar con moléculas ligadas a la superficie del grano.
Estos fotones entrantes pueden también golpear las moléculas del hielo justo en la fase de gas, dice Louis Allamandola de la división astroquímica de NASA-Ames. “La energía entra, y es como golpear algo con un martillo”, comenta. “Y la forma de deshacerse de parte de esa energía, dado que el grano es tan pequeño, es que salgan disparados”.
Los radicales — especies que son reactivas debido a que tienen electrones desparejados — y los iones pueden formarse y acumularse en el hielo o salir disparados y ayudar a formar moléculas mayores.
Cuánta complejidad surge a partir de las colisiones entre gases frente a la química de granos de hielo es un tema de debate, dice Herbst. El trabajo sugiere que el hielo es donde se inicia una gran cantidad de reacciones: los radicales cargados positiva o negativamente pueden ser liberados de esos hielos si la temperatura aumenta, digamos por una explosión cercana o el aumento gradual de calor de una estrella en desarrollo. Estas moléculas entonces pueden también emparejarse, aunque los científicos están lejos de desvelar esta red química.
El modelado se hace incluso más complejo conforme aumentan las temperaturas y cuando se incrementan las poblaciones químicas y el número de reacciones. Teorías, conjeturas, experimentos de laboratorio y comparaciones con las medidas reales del espacio significan constantes ajustes, adición de mejores cifras y re-ejecuciones de experimentos y modelos. Se ayudará a la comprensión completa del paisaje químico cósmico desde otros campos, incluyendo la combustión y la ciencia atmosférica (que están años luz por delante de la astroquímica tanto en teoría como experimentación).
Se dará un gran paso adelante cuando telescopios como ALMA, el Gran Conjunto Milimétrico/Submilimétrico de Atacama, entren en funcionamiento. Reuniendo 66 telescopios en el norte de Chile, ALMA debería estar a pleno funcionamiento para 2013. Estos telescopios permitirán a los científicos estudiar la distribución de las especies moleculares a mayores resoluciones y ver dónde están en relación entre sí. Es como si las actuales tecnologías permitieran a los científicos identificar muchas moléculas en Texas, mientras que los conjuntos harán posible discernir qué está sucediendo en Dallas o Houston.
“La esperanza real es que pronto seremos capaces de tener esta correlación espacial”, dice Pate, “donde realmente podemos decir que parece que la molécula A está siendo consumida y la molécula B está en formación”.
Finalmente, los químicos pueden ser capaces de predecir cómo evolucionan las moléculas de un entorno cósmico u otro. Por ejemplo, las especies asociadas con los granos de hielo pueden liberarse cuando una onda de choque sacuda el firmamento. Detectar la presencia de tal molécula podría ayudar a aislar y situar los choques a través del tiempo galáctico. “Puedes descubrir un montón de cosas”, dice Herbst. “La temperatura, la presión, cómo de rápido se mueve una nube hacia nosotros o colapsa o se aleja de nosotros, o todo lo anterior”.
Alegre animación
Dado que muchas de estas moléculas quedan enbotelladas en cometas y meteroitos y son llevadas a las superficies planetarias, comprender la química cósmica puede llevar a una mejor comprensión del origen de la vida. Los estudios de laboratorio ha generado uracilo, un bloque básico del ARN, a partir de hielos irradiados, según informaron Sandford y sus colegas el año pasado. En 2008, unos investigadores encontraron aminoacetonitrilo, un precursor del aminoácido natural más simple, en el espacio.
La misma radiación ionizante que da a muchos de los festivos radicales espaciales su animación puede también haber dado a la vida su chispa. “Esto entra en el tema de la electricidad – ahora tienes fuerzas eléctricas en lugar de fuerzas químicas”, dice Allamandola. “Una vez que hemos introducido los electrones, pienso en chispas y en Frankenstein”. Sonríe. “Es completamente especulativo, pero podría desempeñar un papel”.
Ya sean creadas en el espacio y llevadas al planeta, o reunidas en algún punto de la joven Tierra, las especies moleculares espaciales es lo que finalmente tenemos. Después de todo, el carbono del universo se creó en el espacio – somos polvo de estrellas.
Nuevas técnicas, telescopios y colaboraciones empujarán a los científicos hacia esta frontera final – y los retará a mantener el ritmo de datos. Cuando ALMA esté operativo, los astrónomos quedarán abrumados por la información. Las mejoras en las técnicas de laboratorio y en el ancho de banda disponible también han aumentado.
“Ahora un año es un día”, dice. “Va a forzar a la gente a pensar distinto sobre cómo observar los datos, analizarlos y extraer la información química. Lo encuentro apasionante. Cuando no me da dolor de cabeza, me apasiona”.
Autor: Rachel Ehrenberg
Fecha Original: 17 de enero de 2010
Enlace Original
____________________________________


















