Capítulo 17.
La genética molecular de los eucariotas
Con la ayuda creciente de las
herramientas de la tecnología del DNA recombinante, progresaron los estudios
de genética molecular de los eucariotas y la distancia entre los eucariotas
y los procariotas, en vez de disminuir, se fue ampliando. En primer lugar, el
cromosoma eucariótico difiere en muchos aspectos del cromosoma procariótico.
Las investigaciones realizadas sobre estos organismos a nivel molecular develaron
también muchas diferencias importantes entre el genoma de los eucariotas
y de los procariotas.
La regulación de la expresión
génica en los procariotas está relacionada fundamentalmente con
el ajuste fino de la maquinaria metabólica de la célula, y es
llevada a cabo activando o reprimiendo la expresión de ciertos genes,
en respuesta a cambios en los nutrientes en el ambiente. La regulación
génica en los eucariotas, especialmente en los multicelulares, es muy
diferente.
Un organismo multicelular usualmente
inicia su vida en forma de huevo fecundado, el cigoto. El cigoto se divide repetidamente
produciendo muchas células que se diferencian y cada tipo celular comienza
a producir proteínas característicamente diferentes que lo distinguen
de otros tipos de células. A su vez, un mismo tipo celular puede producir
variantes de las proteínas que sintetiza en distintas etapas del desarrollo
del organismo. Sin embargo, toda la información genética originalmente
presente en el cigoto también está presente en cada célula
diploide del organismo. Resulta claro que la diferenciación de las células
de un organismo multicelular depende de la inactivación de ciertos grupos
de genes y de la activación de otros, es decir, de una regulación
de la expresión.
La expresión de los genes
puede ser regulada en distintas etapas del camino que conduce desde el DNA a
las proteínas. Las investigaciones en eucariotas han demostrado que,
como en el caso de los procariotas, el genoma eucariótico contiene un
sorprendente arreglo de elementos genéticos móviles. El análisis
del cromosoma eucariótico ha revelado que éste también
está sujeto a reordenamientos, deleciones y adiciones.
En ocasiones, las células
escapan a los factores que regulan el crecimiento celular normal. En consecuencia,
las células se multiplican sin control, amontonándose, invadiendo
y destruyendo otros tejidos. En estos casos se produce el cáncer. Hay
varias evidencias que han relacionado el desarrollo del cáncer con cambios
en el material genético. Los virus pueden provocar cambios en la constitución
genética de la célula y algunos pueden causar cáncer. Más
aun, todos los virus conocidos causantes de cáncer son virus que introducen
información en los cromosomas de las células hospedadoras. Estos
incluyen tanto virus con genoma de DNA como retrovirus con genoma de RNA. El
descubrimiento del papel de la transcriptasa inversa forjó el eslabón
crucial entre los retrovirus y los cromosomas de las células eucarióticas.
El mayor anhelo relativo a las
aplicaciones basadas en la tecnología del DNA recombinante es que en
algún tiempo futuro sea posible corregir defectos genéticos sustituyendo
genes "malos " por genes "buenos". Esta es una tarea enormemente
compleja. Requiere primero la preparación de un gen que será captado
por una célula eucariótica, incorporado a un cromosoma, y luego
expresado, pero esto es sólo el comienzo. El nuevo gen debe establecerse
en un gran número de células del tipo apropiado y quedar sujeto
a los complicados, y todavía grandemente desconocidos, controles del
gen normal.
Se han desarrollado técnicas
que permiten la transferencia de genes a células eucarióticas.
Las células se hacen crecer en cultivo en tubos de ensayo y se transfieren
a óvulos fecundados de ratón y de otras especies de mamíferos
y a embriones de Drosophila.
En cada uno de estos casos,
genes extraños han sido incorporados y expresados en el nuevo hospedador.
En los últimos años también se desarrollaron técnicas
que permiten obtener copias idénticas de organismos, los clones.
El cromosoma eucariótico
El DNA eucariótico siempre está asociado con proteínas, que constituyen más de la mitad del peso del cromosoma. La mayoría de estas proteínas son histonas, moléculas relativamente pequeñas con carga positiva. La molécula de DNA se envuelve alrededor de núcleos formados por ocho moléculas de histonas, para formar nucleosomas, las unidades de empaquetamiento básico del DNA de los eucariotas. Los nucleosomas se empaquetan unos sobre otros formando una estructura más condensada -la fibra de 30 nanómetros- que se encuentra tanto en la cromatina en la etapa de interfase como en los cromosomas que entran en mitosis. El DNA puede tomar in vitro la forma de B-DNA (la hélice dextrógira descrita por Watson y Crick), A-DNA (una hélice dextrógira menos fuertemente enrollada) o Z-DNA (una hélice levógira). Las distintas formas del DNA podrían coexistir in vivo, con distintas funciones biológicas.

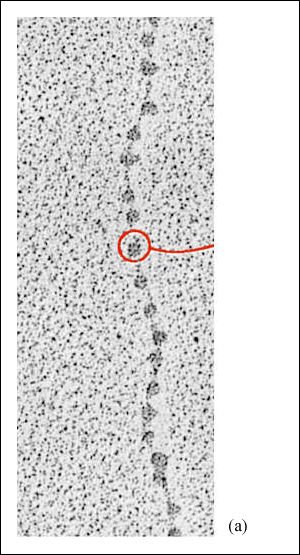
a) Cromatina que se ha descondensado para mostrar los nucleosomas a modo de cuentas.
La distancia entre los nucleosomas es entre 10 y 11 nanómetros y el diámetro
de cada cuenta es aproximadamente de 7 nanómetros. El centro de cada
nucleosoma está compuesto por alrededor de 140 pares de bases de DNA
y un conjunto de ocho moléculas de histona. La cadena que une los núcleos
de los nucleosomas contiene otros 30 ó 60 pares de bases.
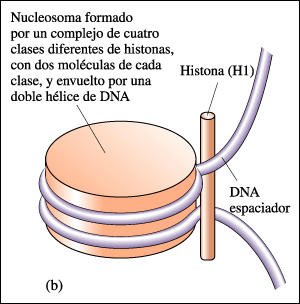
b) Estructura de un nucleosoma. El DNA negativamente cargado se enrolla dos veces alrededor de un centro de proteínas cargadas positivamente. Una molécula de histona Hl (también cargada positivamente) se une a la superficie externa del nucleosoma.
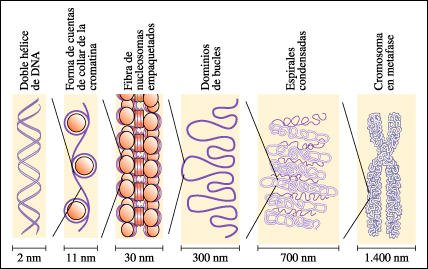
Etapas en el plegamiento de un cromosoma, según varios modelos.
La replicación del DNA
en los eucariotas es igual, en principio, a la replicación del DNA de
los procariotas. Los nucleótidos en la forma de trifosfatos se acoplan
a lo largo de una cadena molde de DNA en la forma semiconservativa. Como en
los procariotas, en la síntesis de las cadenas complementarias, las DNA
polimerasas operan solamente en una dirección''; la cadena complementaria
a la otra hebra madre ''se sintetiza como una serie de fragmentos de Okazaki,
que luego se unen por la acción de la enzima DNA ligasa.
En el cromosoma procariótico
circular, comparativamente pequeño, la replicación comienza en
un único origen y procede bidireccionalmente a lo largo de dos horquillas
de replicación.
Las histonas ensambladas en
los nucleosomas raramente se separan del DNA, por lo tanto, a medida que la
horquilla de replicación avanza debe, de alguna manera, pasar a través
de los nucleosomas parentales. Se cree que cada nucleosoma se desenrolla transitoriamente,
permitiendo que la DNA polimerasa copie el DNA nucleosomal desenrollado. El
DNA recién sintetizado hereda parte de las viejas histonas pero requiere
también de nuevas histonas para empaquetarse y formar la cromatina. En
cuanto se sintetiza, el DNA eucariótico forma los nucleosomas y se asocia
también con otras proteínas compactándose en los niveles
superiores de condensación.
El genoma eucariótico
El examen del DNA de las células
eucarióticas reveló cuatro sorpresas principales. En primer lugar,
con algunas pocas excepciones, en una misma especie, los individuos tienen la
misma cantidad de DNA en cada una de sus células diploides (lo cual no
es sorprendente), pero las variaciones entre las diferentes especies son enormes.
En segundo lugar, en cada célula
eucariótica parece haber un gran exceso de DNA, o por lo menos de DNA
cuyas funciones son desconocidas. Se estima que en las células eucarióticas
menos del 10% de todo el DNA codifica para proteínas; en los seres humanos,
esta cifra puede disminuir hasta el 1%. Por contraste en los procariotas y más
aun en los virus, excepto por las secuencias reguladoras o secuencias señal,
virtualmente todo el DNA se expresa.
En tercer lugar, casi la mitad
del DNA de la célula eucariótica consiste en secuencias de nucleótidos
que se repiten centenas, o hasta millones de veces. Esto fue un descubrimiento
particularmente sorprendente. En E. coli, que ha sido por largo tiempo el modelo
para los genetistas moleculares, cada molécula de DNA cromosómico
contiene típicamente sólo una copia de cualquier gen dado; las
principales excepciones son los genes que codifican los RNA ribosómicos.
Además, este hallazgo fue sorprendente porque, de acuerdo con la genética
mendeliana, un gen está presente solamente dos veces por cada célula
encariótica diploide, no en una multitud de copias. Los estudios de hibridación
y secuenciación han mostrado tres clases de DNA eucariótico. Las
repeticiones múltiples de secuencias de nucleótidos cortas, dispuestas
característicamente en tándem, se conocen como DNA de secuencia
simple. El DNA de secuencia simple está asociado con la heterocromatina
fuertemente condensada en la región del centrómero. Las repeticiones
más largas, habitualmente dispersas en el cromosoma, se conocen como
DNA de repetición intermedia. El DNA de repetición intermedia
incluye múltiples copias de los genes que codifican para los RNA ribosomal,
RNA de transferencia e histonas. La tercera clase, el DNA de copia única,
constituye hasta el 70% del DNA cromosómico en los seres humanos y dentro
de esta fracción se encuentra el DNA que codifica para la mayor parte
de las proteínas. Los datos actuales indican que sólo un 1% del
genoma humano puede traducirse a proteína.
La cuarta sorpresa, y tal vez
la más inesperada de todas, fue que las secuencias de genes eucarióticos
que codifican para proteínas habitualmente no son continuas, sino que
están interrumpidas por secuencias no codificadoras.
Las secuencias no codificadoras
que producen interrupciones dentro de un gen se conocen como secuencias interpuestas
o intrones, y las secuencias codificadoras, aquellas que se expresan, son llamadas
exones.
Aunque los intrones se transcriben
a RNA en el núcleo, no están presentes en el mRNA en el citoplasma
y, así, no se traducen a proteínas. Los exones son los segmentos
que están presentes en el mRNA citoplásmico y que se traducen
a proteína.
Algunos genes estructurales,
como los que codifican para las cadenas polipeptídicas de las moléculas
de hemoglobina, forman familias génicas. Los genes individuales de la
familia difieren ligeramente en sus secuencias de nucleótidos; en consecuencia,
las proteínas que ellos codifican difieren ligeramente en estructura
y en propiedades biológicas. Algunos miembros de las familias génicas
no se expresan, supuestamente a raíz de mutaciones deletéreas;
estas secuencias de DNA se conocen como pseudogenes. Se cree que las familias
génicas tienen sus orígenes en duplicaciones génicas que
ocurrieron como resultado de "errores" de recombinación, seguidos
por diferentes mutaciones en diferentes copias del gen.
La regulación de la expresión
génica en los eucariotas
Los biólogos están
comenzando a comprender algunos aspectos de la regulación de la expresión
génica en eucariotas. Durante el desarrollo embrionario, diferentes grupos
de genes se activan o inactivan en diferentes tipos de células. Una variedad
de proteínas reguladoras específicas desempeñan papeles
centrales en la regulación de la expresión génica. Para
poder iniciar la transcripción, la RNA polimerasa requiere que un grupo
de proteínas, llamadas factores generales de transcripción, se
ensamblen en la región promotora del gen que se va a transcribir. Esto
permite la unión de la RNA polimerasa y la posterior transcripción.
Si bien en los procariotas también
se da una regulación a este nivel, se hace cada vez más claro
que este nivel de control de la transcripción es mucho más complejo
en los eucariotas, en particular, en los multicelulares. En un organismo multicelular,
un gen parece responder a la suma de muchas proteínas regulatorias diferentes,
algunas de las cuales tienden a activar el gen y otras a desactivarlo. Los sitios
en los cuales se unen esas proteínas regulatorias pueden estar a centenares
o miles de pares de bases de distancia de la secuencia promotora en la que se
une la RNA polimerasa. Entre estas secuencias regulatorias, se cuentan las secuencias
denominadas enhancers, a las que se unen las proteínas que activan la
transcripción.
Muchas evidencias indican que
el grado de condensación del DNA del cromosoma, que se observa mediante
la tinción de la cromatina, desempeña un papel principal en la
regulación de la expresión génica en las células
eucarióticas. La tinción revela dos tipos de cromatina: la eucromatina
y la heterocromatina. Durante la interfase, la heterocromatina permanece condensada,
pero la eucromatina se vuelve más laxa. La transcripción del DNA
a RNA ocurre solamente durante la interfase, cuando la eucromatina está
laxa.
Algunas regiones heterocromáticas
son constantes de célula a célula y nunca se expresan. Este tipo
de heterocromatina se denomina heterocromatina constitutiva. Un ejemplo es la
cromatina altamente condensada, localizada en la región del centrómero
del cromosoma. Esta región, que no codifica para proteínas, desempeña
un papel estructural en el movimiento de los cromosomas durante la mitosis y
la meiosis.
Otras regiones de cromatina
condensada, por el contrario, varían de un tipo de célula a otro
dentro del mismo organismo, reflejando la biosíntesis de diferentes proteínas
por diferentes tipos de células. Además, cuando las células
se diferencian durante el desarrollo embrionario, la proporción de heterocromatina
aumenta respecto de la de eucromatina a medida que la célula se vuelve
más especializada.
Otro factor que está
involucrado en la regulación génica es la metilación de
las bases nitrogenadas citosinas, que ocurre después de la replicación.
La metilación diferencial de ciertos genes en ambos sexos, que ocurre
durante la gametogénesis, la impronta genómica, desempeña
un papel en el desarrollo temprano del embrión.
Transcripción, procesamiento
de mRNA y síntesis de proteínas en eucariotas
Una célula eucariota
regula las proteínas que sintetiza controlando:
1) el momento y la frecuencia
con que un determinado gen es transcripto (control transcripcional);
2) el procesamiento del mRNA
transcripto (control de procesamiento de mRNA);
3) las moléculas de mRNA
que son exportadas del núcleo al citoplasma (control de transporte del
mRNA);
4) los mRNA que son traducidos
por los ribosomas en el citoplasma (control de traducción);
5) la vida media del mRNA (control
de degradación del mRNA) y
6) la activación e inactivación
de proteínas (control de la actividad de las proteínas). De todas
estas etapas de regulación, la primera es la que resulta más económica
para la célula. La transcripción en los eucariotas difiere de
la de los procariotas en varios aspectos.
En la transcripción de los eucariotas están implicadas tres RNA polimerasas diferentes, cada una especializada en transcribir distintos tipos de genes. Además, se requieren factores generales de transcripción, que permiten la unión de las RNA polimerasas al promotor, así como una multiplicidad de proteínas regulatorias. Además, en los eucariotas los genes estructurales no están agrupados en operones como lo están frecuentemente en los procariotas; la transcripción de cada gen se regula por separado y cada gen produce un transcripto de RNA que contiene la información codificada de un solo producto. Los transcriptos de RNA se procesan en el núcleo y producen las moléculas maduras de mRNA que pasan al citoplasma a través de los poros nucleares. Este procesamiento incluye la adición de un casquete de metilguanina (CAP) al extremo 5' de la molécula y de una cola de poli-A al extremo 3', así como la remoción de los intrones, en un proceso conocido como empalme o "splicing". El empalme alternativo de transcriptos de RNA idénticos en diferentes tipos de células puede producir diferentes moléculas de mRNA maduro que se traducen en diferentes polipéptidos.
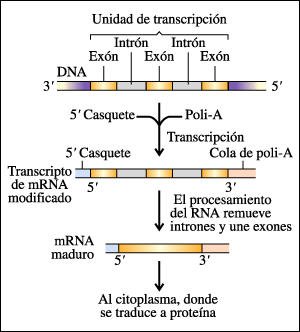
Resumen de las etapas en el procesamiento del mRNA transcripto a partir de genes estructurales de los eucariotas.
La información genética
codificada en el DNA se transcribe a una copia de RNA (transcripto primario).
Esta copia luego se modifica con la adición del casquete 5' (CAP) y la
cola de poli-A, la escisión de los intrones y la unión de los
exones (splicing). El mRNA maduro luego va al citoplasma, donde se traduce a
proteínas.
La traducción a proteínas es similar a la de procariotas, con
algunas diferencias en el reconocimiento de los mRNA por los ribosomas, en la
formación del complejo de iniciación y en el número de
factores proteicos que participan en la iniciación, elongación
y terminación. La síntesis de proteínas comienza siempre
en ribosomas libres en el citosol y señales presentes en la cadena polipeptídica
determinan las modificaciones posteriores y su localización final. Las
proteínas destinadas al sistema de endomembranas (retículo endoplásmico,
complejo de Golgi o lisosomas), a la membrana plasmática o de exportación
se sintetizan en ribosomas que se asocian transitoriamente a membrana del retículo
endoplásmico y son translocadas al lúmen donde se les agrega una
cadena corta de azúcares. La glucosilación de las proteínas
finaliza en el complejo de Golgi, donde son clasificadas y empaquetadas en vesículas
que las conducen a su localización final.
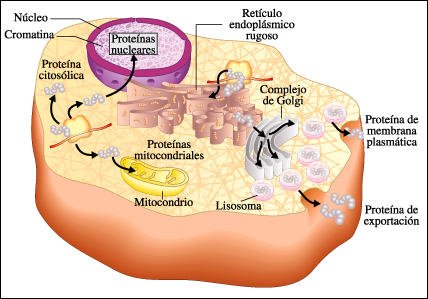
Resumen del camino de algunas de las proteínas que se sintetizan en el retículo endoplásmico rugoso o en ribosomas libres. En esta figura, los ribosomas en los que se están sintetizando proteínas no estan dibujados a escala (en realidad son mucho mas chicos, como los que se muestran sobre el REG).
Genes en movimiento
Hay genes que se mueven hacia
adentro y hacia afuera del genoma bacteriano, afectando tanto su estructura
como su función. El análisis del cromosoma eucariótico
ha revelado que éste también está sujeto a reordenamientos
que afectan tanto su estructura como su función.
Los genes funcionales de anticuerpos se forman durante la diferenciación de los linfocitos por el reordenamiento de secuencias génicas que codifican para diferentes partes de la molécula del anticuerpo. Los virus, que incluyen tanto a los virus con genoma de DNA como a los retrovirus con genoma de RNA, pueden integrarse al cromosoma eucariótico; entonces se conocen como provirus. La incorporación de la información genética llevada por los retrovirus con genoma de RNA depende de la transcripción del RNA a DNA, que está catalizada por la transcriptasa inversa. Los transposones eucarióticos se asemejan a los de los procariotas en que, al insertarse en el genoma, activan o inactivan genes, ya sea interrumpiendo las secuencias codificadoras o interfiriendo con la regulación. Como en los procariotas, los transposones pueden no moverse en realidad, sino generar una copia que se integra en otro lugar del genoma. Muchos transposones eucarióticos, los retrotransposones, difieren más notablemente de los de los procariotas en que primero se transcriben a RNA y luego nuevamente a DNA, antes de insertarse en otro sitio del cromosoma.
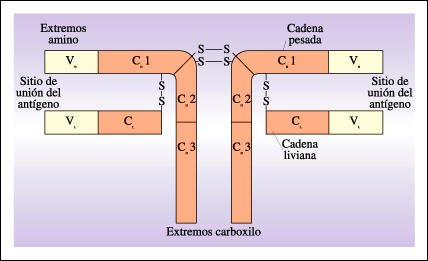
Estructura de una molécula de anticuerpo.
La molécula de anticuerpo tiene dos cadenas polipeptídicas livianas (L) y dos cadenas pesadas (H), cada una de las cuales tiene una región variable (V) (en color amarillo) y una región constante (C) (en color rosa). Las cadenas polipeptídicas se conectan entre sí por puentes disulfuro (S-S). Las regiones variables de las cadenas livianas y pesadas forman una estructura tridimensional compleja, que es la porción de la molécula de anticuerpo que reconoce a los antígenos extraños y se une a ellos.
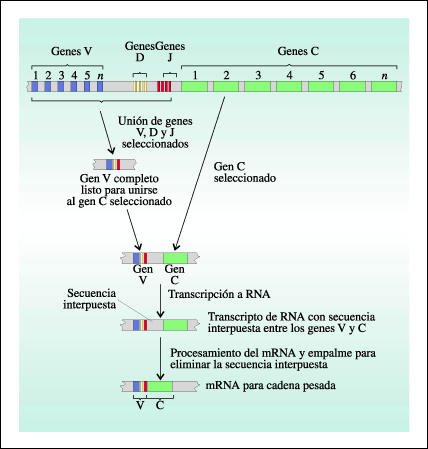
Representación esquemática del ensamble de los genes que codifican una cadena pesada de anticuerpo.
Los genes variables (V), de diversidad (D) y de unión (J) seleccionados son transpuestos de diferentes regiones del cromosoma para formar un gen variable completo, que luego se une a uno de los genes constantes (C). La secuencia interpuesta (intrón) entre las secuencias constante y variable se elimina del transcripto de RNA para dar la molécula de mRNA terminada.
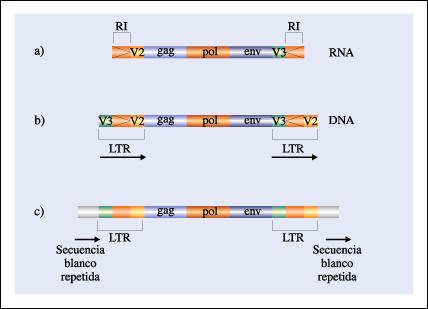
Esquema del genoma de un retrovirus.
En a) se muestra el RNA viral, con los genes gag, pol y env que codifican respectivamente para las proteínas de la cápside, la transcriptasa inversa y las proteína de envoltura. Los extremos terminales son secuencias con repeticiones invertidas. Cuando el RNA viral se copia a DNA (b), los extremos forman las repeticiones terminales largas (LTR). c) Al integrarse al genoma de la célula hospedadora (provirus), se produce una duplicación de la secuencia blanco en el sitio de inserción.
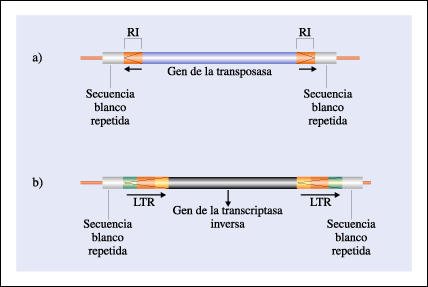
Esquema de un transposón y un retrotransposón eucarióticos.
a. Transposón cuya región
central es una secuencia de DNA, a menudo de varios miles de pares de bases
de longitud, que contiene un gen que codifica para la transposasa (la enzima
que inserta el transposón en el cromosoma hospedador, cortando y empalmando
el DNA hospedador). Este segmento también puede llevar otros genes que
codifican para otras proteínas. Los genes centrales están flanqueados
por repeticiones invertidas (R1) que son imágenes especulares; si una,
por ejemplo, es AATG, la otra será GTAA. Las repeticiones invertidas
son la secuencia de reconocimiento para las transposasas.
b. Retrotransposón. La
región central contiene un gen que codifica para la transcriptasa inversa.
Está flanqueado por repeticiones terminales largas (LTR) directas. Las
repeticiones directas son copias de un segmento corto (de 5 a 10 pares de bases)
del DNA hospedador.
Genes, virus y cáncer
Hay varias evidencias que han
relacionado durante mucho tiempo el desarrollo del cáncer con cambios
en el material genético. Primero, una vez que una célula se ha
transformado en cancerosa, todas las células hijas son cancerosas; en
otras palabras, el cáncer es una propiedad heredada de las células.
Segundo, anormalidades cromosómicas, como deleciones y translocaciones,
son frecuentemente visibles en las células cancerosas. Tercero, la mayoría
de los carcinógenos (agentes que se sabe que causan cáncer, como
los rayos X, la radiación ultravioleta, el humo del tabaco y una variedad
de productos químicos) son también mutágenos.
El cáncer se considera
a menudo un grupo de enfermedades antes que una única enfermedad porque,
con pocas excepciones, cualesquiera de los 200 o más tipos celulares
del cuerpo humano puede transformarse en un tejido maligno. El comportamiento
de las células y el pronóstico de la enfermedad dependen del tipo
de células que se hayan transformado en malignas.
Las técnicas de DNA recombinante
han permitido a los biólogos moleculares estudiar algunos de los cambios
de los cromosomas eucarióticos que llevan al cáncer. Estos estudios
habitualmente se llevan a cabo en células que crecen en cultivos de tejido.
Cuando estas células se exponen a un agente cancerígeno, como
un virus, pueden sufrir cambios característicos en sus patrones de crecimiento
y en su forma. Se dice que esas células han sufrido una transformación.
Las células transformadas pueden producir cánceres cuando se transplantan
a animales de laboratorio. Estudios de células transformadas han descubierto
un grupo de genes conocidos como oncogenes. Los oncogenes (genes c-onc) se asemejan
mucho a ciertos genes normales (protooncogenes) de las células eucarióticas
en las cuales se encuentran. De acuerdo con la hipótesis del oncogén,
el cáncer es causado cuando algo funciona mal en la expresión
de estos protooncogenes celulares normales, como resultado de mutaciones en
los propios genes, cambios en la regulación génica, o ambos. Cuando
el protooncogen está alterado en alguno de esos modos, se denomina oncogén.
Todos los virus conocidos causantes
de cáncer son virus que introducen información en los cromosomas
de las células hospedadoras. Los virus pueden causar cáncer de
tres maneras diferentes. Primero, simplemente por su presencia en el cromosoma,
los virus pueden alterar la función de los genes normales. Segundo, los
virus pueden codificar proteínas necesarias para la replicación
viral que también afecten la regulación del ciclo celular.Tercero,
algunos retrovirus pueden servir como vectores de oncogenes. De hecho, los oncogenes
se descubrieron cuando el análisis genético de retrovirus causantes
de cáncer reveló la presencia de genes que los virus no necesitaban
para su propia multiplicación. Se encontró posteriormente que
las secuencias de nucleótidos de estos oncogenes virales (llamados v-onc)
son equivalentes a algunos oncogenes que se encuentran en células tumorales
(c-onc) y también causan la transformación maligna de las células.
La estrecha vinculación entre los genes c-onc y los v-onc denota el origen
de estos últimos que, probablemente, hayan sido capturados por el genoma
viral del genoma de la célula hospedadora.
Hasta el momento se han descubierto
aproximadamente 50 oncogenes. Sus productos génicos identificados son
proteínas reguladoras, implicadas en el control del crecimiento celular
o bien de la división celular. El estudio de los oncogenes no sólo
nos está acercando al control de uno de nuestros más viejos y
desagradables enemigos, sino que también está produciendo nueva
información acerca de la cuestión fundamental de la regulación
del crecimiento celular.
Transferencia de genes entre
células eucarióticas
La transferencia de genes entre
células comenzó cuando se quizo lograr que el genoma de las células
eucarióticas incorporara en forma estable un DNA extraño y que
éste se expresara en ellas. En el primer experimento de este tipo, se
usó un virus como vector.
Posteriormente se encontró
que, al exponer las células en cultivo a DNA purificado, precipitado
con ion calcio (Ca2+), se estimula la captación de DNA. Aparentemente,
algunas células (aproximadamente una en un millón) fagocitan el
precipitado e incorporan el DNA. Pero surge el problema de identificar y seleccionar
las células que han incorporado a su genoma el DNA extraño.
Existen métodos que facilitan
la selección de las células que han incorporado el DNA extraño.
En general, todos se basan en introducir en las células el gen extraño
junto con un gen llamado "gen marcador". La incorporación y
expresión del gen marcador, que puede ser un gen de resistencia a un
antibiótico, confiere a las células la capacidad de crecer en
un medio selectivo que frena el crecimiento de las células que no han
incorporado el DNA.
Actualmente, la transferencia
de DNA a células eucarióticas en cultivo, transfección,
se realiza por varios métodos.
El desarrollo exitoso de técnicas
para introducir genes en células en cultivo abrió nuevas posibilidades
que llevaron al desarrollo de metodologías que permitieron introducir
genes en animales. Esta idea se convirtió en realidad. Un animal que
incorpora información genética nueva, por agregado de DNA extraño,
se denomina transgénico y el gen incorporado se denomina transgén.
Por medio de la técnica
de microinyección, se introdujeron genes extraños en óvulos
fecundados. Esos genes extraños introducidos se han expresado en los
organismos que se desarrollaron a partir de esos óvulos.
Por ejemplo, se combinó el gen de la hormona de crecimiento somatotropina humana con la porción reguladora de un gen de ratón y se inyectó en óvulos fecundados de ratón. Los ratones transgénicos resultantes crecieron hasta el doble del tamaño normal, indicando que el gen humano se había incorporado al genoma del ratón y estaba produciendo hormona de crecimiento. Dado que el DNA se había inyectado en los óvulos, apareció en todas las células, incluyendo las células germinales, y así pudo ser transmitido a la generación siguiente.
Estas dos hembras de ratón, son crías pequeñas de la misma camada. El óvulo fecundado del que se desarrolló la hembra de la izquierda fue inyectado con un gen que consistía en las secuencias promotora y reguladora de un gen de ratón combinadas con el gen estructural de la hormona de crecimiento humana.
Después de la integración,
el nuevo gen en el genoma de la hembra de ratón de la figura anterior
se transmitió a su progenie. En promedio, los ratones que expresan el
nuevo gen crecen de 2 a 3 veces más rápido que los ratones que
carecen de él y, como adultos, tienen el doble del tamaño normal.
Este tipo de procedimiento ha
sido llevado a cabo con varios genes clonados. En general, la incorporación
del gen extraño se produce por recombinación en sitios al azar.
En uno de cada mil de esos eventos, el gen extraño reemplaza a su homólogo
en el genoma receptor por recombinación homóloga. Del 10 al 30%
de los óvulos fecundados sobrevive a la manipulación y el gen
extraño funciona en un 40% de este porcentaje. La técnica de microinyección
de DNA directamente en óvulos fecundados tiene por lo tanto limitaciones.
Posteriormente, fue desarrollada
en ratones una metodología alternativa para introducir genes en embriones
en desarrollo. Se encontró que células de un embrión temprano
de ratón, en estado de blastocisto, podían proliferar en un cultivo
realizado in vitro. Estas células especiales, denominadas células
embrionarias totipotenciales (ES), pueden ser mantenidas en cultivo en condiciones
adecuadas que evitan su diferenciación. Si son reintroducidas en un blastocisto,
se diferencian y contribuyen al desarrollo del organismo participando en la
formación de los tejidos. Aprovechando la capacidad de estas células
embrionarias de mantener sus características en cultivo, se puede introducir
en su genoma DNA extraño por los métodos de transfección.
Esta metodología permite
la introdución de modificaciones mucho más específicas
y es, por lo tanto, mucho más eficiente que la microinyección
en el desarrollo de ratones transgénicos.
El desarrollo de animales transgénicos
hizo posible abordar el estudio en mamíferos de la expresión diferencial
de genes en distintos tejidos durante el desarrollo, establecer modelos para
el estudio de enfermedades humanas y probar potenciales agentes terapéuticos.
Una de las alternativas interesantes es el uso de animales transgénicos
como biorreactores para la producción de proteínas farmacológicamente
importantes de uso humano. La fusión del gen extraño con un fragmento
de DNA que contiene la región regulatoria de una proteína que
normalmente está presente en la leche del animal permite que el gen de
interés se exprese específicamente en la glándula mamaria
del animal transgénico y que su producto proteico se secrete en la leche.
Recientemente se ha desarrollado
en mamíferos una metodología que permite obtener clones de animales.
Esta metodología se basa en la transferencia del núcleo de una
célula en cultivo a un ovocito no fecundado al cual previamente se le
extrajo su material genético. El ovocito anucleado es sometido a un pulso
de corriente que simula la estimulación que proporciona el espermatozoide
y se fusiona con la célula dadora del núcleo. Algunos de los ovocitos
fusionados comienzan a desarrollarse como un embrión normal y son implantados
en una madre sustituta. En los primeros ensayos, realizados en ovejas, las células
dadoras del núcleo fueron células de embriones tempranos (9 días)
en cultivo. Los ovocitos que recibieron el núcleo de estas células
se desarrollaron en organismos adultos. Más recientemente, se realizó
con éxito el mismo procedimiento con células somáticas
en cultivo de una oveja adulta. De este experimento nació Dolly, el primer
mamífero clonado a partir de un adulto. El éxito de esta metodología
se basa en coordinar los ciclos de replicación del DNA y los de producción
de mRNA de ambas células. Para esto, las células dadoras del núcleo
son cultivadas, previo a la fusión, en un medio con escasa cantidad de
nutrientes, que lleva a las células a mantenerse en las fases G0 o G1
del ciclo celular , en las cuales no hay replicación de DNA. De este
modo, durante las primeras divisiones del embrión en desarrollo, se expresarán
únicamente las proteínas codificadas por el mRNA presente en el
citoplasma del ovocito. Esto permite la reprogramación del núcleo
por interacción con las proteínas regulatorias del ovocito receptor.
La posibilidad de obtener clones a partir de células en cultivo facilita el desarrollo de animales genéticamente modificados (transgénicos). La ventaja de esta técnica respecto a la de la microinyección es la mayor eficiencia en la obtención de animales transgénicos y la posibilidad de crear múltiples "copias génicas" de organismos portadores de la misma modificación genética.
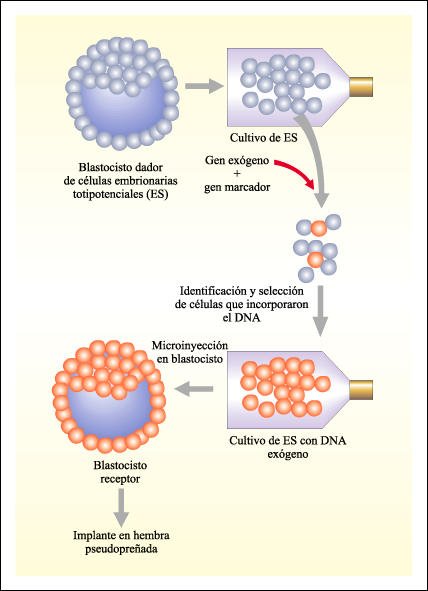
Metodología para introducir genes en embriones en desarrollo
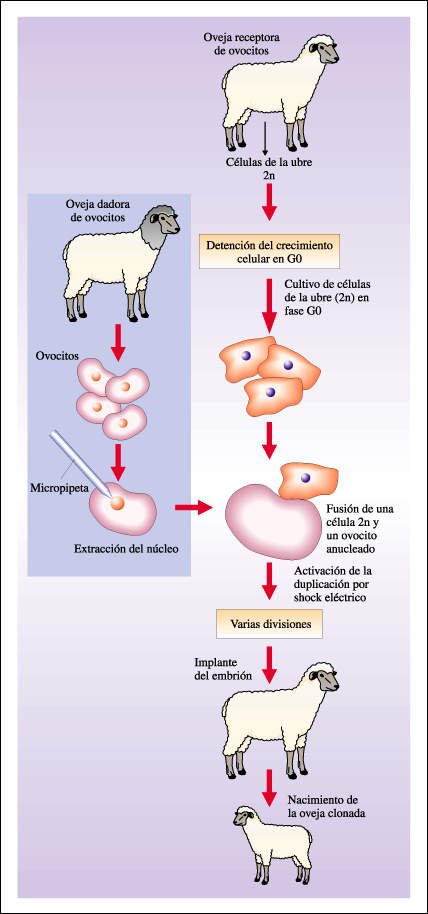
Esquema del proceso que permitió clonar un mamífero a partir de una célula adulta.
También se ha realizado
en forma muy exitosa la transferencia de genes usando transposones a embriones
de Drosophila. Estos son los primeros indicios de que los transposones podrían
convertirse en vectores útiles.